Ex Vivo试验用于药效评估案例分享和难点分析

前 言
随着国家药品监督管理局药品审评中心正式发布《以临床价值为导向的抗肿瘤药物临床研发指导原则》,中国的新药研发迈入深水区。当以患者为核心的临床药物研发开展新药临床试验设计时,对照组由普遍安慰剂变成了广泛应用的最佳治疗方式/药物,创新药临床研发和获批的规则正在被深刻的改变,同时新药物获批难度将会进一步增大。临床试验阶段,新药是否有效?将会被新药是否比现有疗法/同类药物更加有效这个问题所替代。临床试验检测过程中越早对有效性的问题进行回答,在现有的政策环境下越能够加快临床的进度,或者及时规避风险。使用Ex Vivo试验用于早期临床特别是一期临床的药效学评估,是新药特别是First in class新药常用的评估方式。笔者将从检测原理,案例分析和熙宁生物的临床检测实践三方面对Ex Vivo试验用于早期临床的药效学评估进行论述。
Ex Vivo试验用于临床检测原理
有别于In-Vitro(体外试验)使用的活性蛋白或者肿瘤细胞系,In-Vivo(体内试验)使用动物或者人体,Ex Vivo(离体试验)使用的从动物/人体取出的原代细胞/组织,采用体外试验的模式进行检测分析。
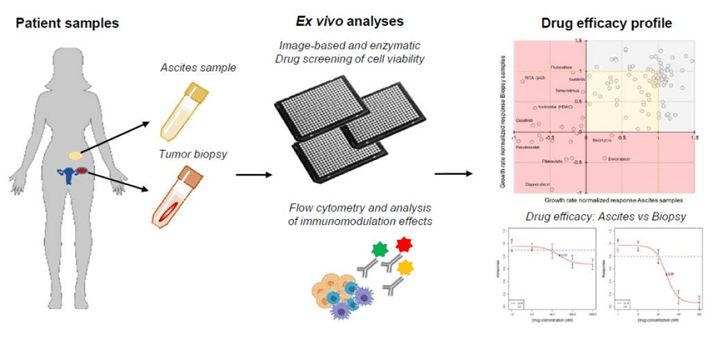
临床Ex Vivo试验模式由于其使用的材料来自于用药后的人体,该检测方法相对于In-Vitro试验来说,能够较为真实的还原药物在人体复杂免疫细胞互作环境下的真实表现,更具备生理相关性。同时,临床Ex Vivo试验使用体外检测的模式,相对于In-Vivo试验,试验周期较短,能够更为快捷得到有参考价值的数据,特别是在临床一期健康受试者的临床试验中,基于药物的作用机理,通过设计合适的Ex Vivo评价方案,可以获得跟药物作用机理紧密相关的药效学数据。
临床Ex Vivo试验多采用能够通过较为简单方式从人体获得的生物材料,通常为人全血,人PBMC或者人血清。使用人体的生物材料进行检测,样品具备多重属性,既包含有药物成分,也作为检测体系中重要构成材料,且存在个体差异,不同采样点的状态差异等,临床Ex Vivo试验的样品采集条件控制,检测条件控制,数据处理和解读均较为复杂,是难度和变异系数最高的检测实验类型。
无论是小分子药物,抗体类药物,免疫调节剂类药物,疫苗类药物均可通过使用人全血中特定的细胞亚群或者组分,直接进行或者作为替代标志物进行药效学评估。
Ex Vivo试验临床早期进行
药效学检测案例分析
随着中国新药研发进一步加速,药物研发模式完成了由药物仿制到靶点追踪模式的转变,随着监管政策的进一步收紧,药物研发模式必将进一步进行优化。笔者认为后续新药研发模式进一步优化,其中一个重要环节在于临床药物评价体系的构建,使用Ex Vivo试验临床早期进行药效学检测评估将会使临床药物评价体系中重要一环,下面笔者通过公开的资料梳理下Ex Vivo试验用于早期药效学评估的案例。
案例1:抗体药物Zolbetuximab(anti-Claudin18.2)和cetuximab (anti-EGFR)的Ex Vivo ADCC和CDC功能。
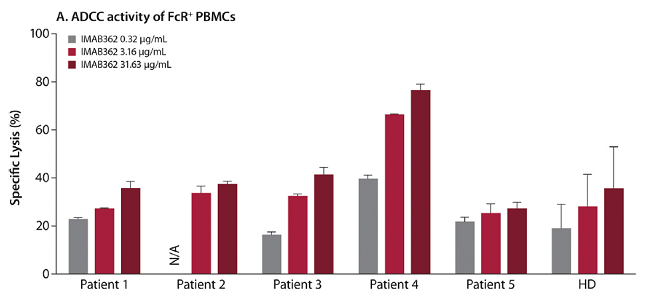
抗体药物通过靶向肿瘤的靶点,介导机体免疫细胞和补体杀伤肿瘤细胞,发挥ADCC和CDC功能是靶向抗体药物的主要的药效学作用机理,在1期临床中进行Ex Vivo ADCC和CDC功能学评估是预测在个体中药物是否能够起效的一个关键指标。使用细胞杀伤模型检测人样品中IMAB362药物介导人样品PBMC介导的杀伤NUGC4的效果,报告基因方法进行检测。


案例2:CD28免疫激动剂Davoceticept (ALPN-202)的Ex Vivo临床药效学评估
使用全血共刺激模型检测人样品中CD28激动剂Davoceticept药物介导全血刺激后IL2的分泌,ELISA方法进行检测。


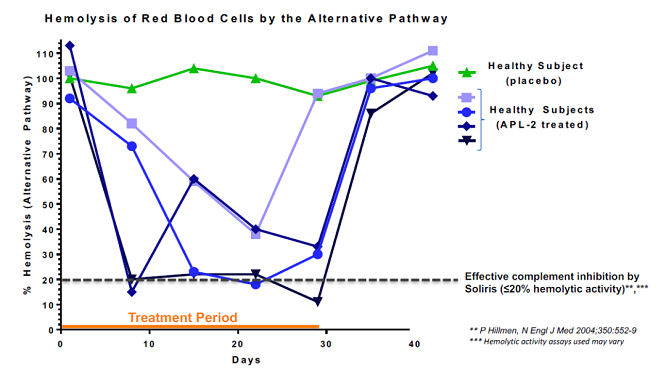
案例3:C3补体抑制剂Empaveli的Ex Vivo临床药效学评估
使用补体旁路活化途径溶血模型检测人样品中Empaveli药物介导的人样品中血清的溶血效果。

案例4:CDK4/6抑制剂Trilaciclib的Ex Vivo临床药效学评估
使用全血刺激模型检测人样品中Trilaciclib介导的对人样品中全血T细胞的增殖抑制效果,流式方法进行检测。


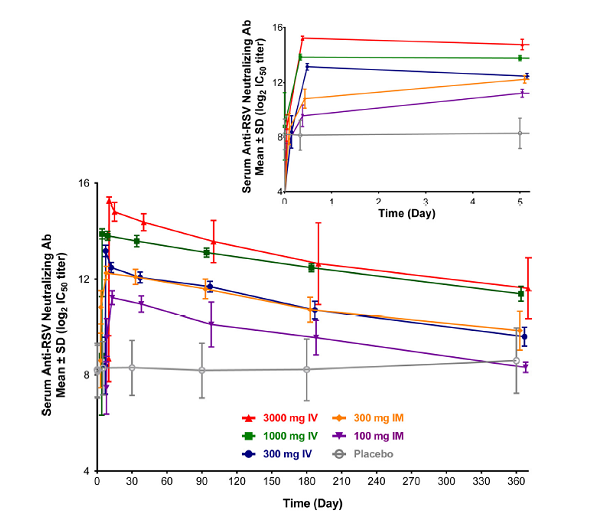
案例5:RSV抗体Nirsevimab的Ex Vivo临床药效学评估

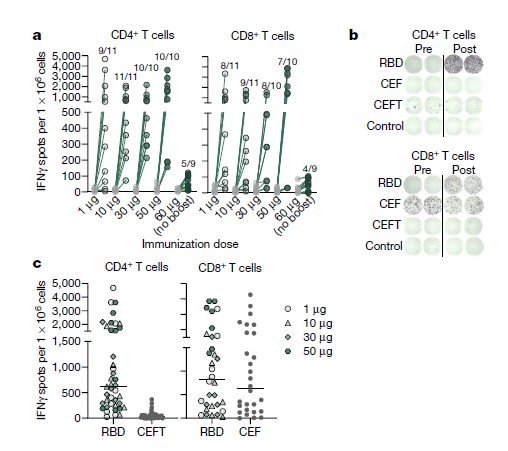
案例6:COVID-19 vaccine BNT162b1的Ex Vivo临床药效学评估
使用COVID-19 Spike蛋白刺激PBMC模型检测Spike蛋白RBD多肽Pool刺激人样品中CD4+和CD8+ T细胞,检测人样品细胞免疫效果,ELISPOT方法进行检测。

案例7:IL-4Ra 抑制剂 AZD1402的Ex Vivo临床药效学评估
使用全血刺激模型检测人样品中AZD1402介导的对人样品中全血CD3细胞的STAT6磷酸化水平抑制效果,流式方法进行检测。

熙宁生物
Ex Vivo试验临床检测实践和难点考量
熙宁生物有非常丰富的小分子药物和生物制品早期临床的药效学评估经验,相对于传统的PK药物代谢,定量型biomarker或者免疫原性分析方法,Ex Vivo药效学试验有包含全部或者部分显著性区别和难点:
1. 非定量型检测。药效学检测的是药物引起体内生物材料的变化如PBMC的转录因子蛋白磷酸化水平变化,该变化指向的目的分子往往没有标准物质,无法在检测体系中建立标准曲线,样品检测无法汇报具体的浓度结果。该情况引发的后果是需要通过检测方法得到信号值变化或者均一化以后的信号值变化来对药物引起的变化进行表征,而在长期的样品分析过程中,信号值变化除了会受到药物的影响,同时也会受到不同天检测方法条件的影响,为多变量参数。因此,在进行Ex Vivo药效学试验时,维持不同天检测方法条件的严格一致性,是临床药效学试验取得跟药物有相关性结果的关键。
2. 个体差异。Ex Vivo药效学试验检测结果除了受药物影响外,会受到来自于个体的生物材料的显著影响,通常生物材料具备显著的个体差异(如不同个体的PBMC在检测体系中有不同的响应强度)。该情况引发的后果是需要通过检测单个个体的Pre-dose样品和用药后样品进行药效学比较,可能会出现不同个体的药效学结果差异较大的情况,如在A个体中药物有效,在B个体中药物无效。个体用药后的药效需要结合个体能够引发的检测体系的响应强度综合进行判断,必要时需要根据个体能够引发的检测体系的响应强度进行分组来分析药物的药效学效果。
3.样品稳定性。Ex Vivo药效学试验的检测样品具备多元属性,样品中的药物为检测物质,样品中的生物材料如全血为检测体系的试剂。通常情况下药物较为稳定,但是作为检测试剂的生物材料并非稳定的存在,全血在检测体系的稳定性通常为48-72小时以内,个别项目要求24小时以内, 甚至为8小时以内,需要进行严格的考察。样品的检测结果由样品的药物浓度和样品的生物材料活性共同决定,在进行样品分析时需要确保样品的生物材料活性出于最佳的状态,这对样品采集,运输和检测时间均有较为严格的要求。同时由于样品需要较短时间内进行分析,会导致Pre-dose,用药后各采血点的样品不能同时在一个分析批进行分析,没有标准曲线的对分析批信号的校准,将会进一步增加检测结果的波动性。
4. 样品刺激体系的建立。通常情况下健康人用药后,样品中的药物对样品中的生物材料无明显的药效学作用,需要对样品中的生物材料进行刺激后,样品中的药物才能显现出药效学。刺激物的选择,刺激时间的选择,检测目的分子和检测平台的选择均需要基于药物的作用机理,生物材料的生理学效应进行设计,一个类型的药物需要一个类型的方法。在进行Ex Vivo药效学试验时样品中生物材料的运输保存和刺激,将会显著性的影响检测结果,是整个分析方法组成的一部分。在进行方法学开发和验证过程中,将药物加入生物材料中配制为模拟样品进行方法学验证,是一个方法是否符合实际应用的关键。
5. 平台和人员熟练度。Ex Vivo药效学试验时通常包括样品的刺激和目的检测分子检测两部分,样品的刺激通常需要进行全血,PBMC等生物材料的处理,由于该类型生物材料的个体差异和稳定性较差,需要有较为丰富经验的人员。同时不同的药效学方法检测平台不一样,可能会使用如细胞,ELISA,FACS,MSD,ELISPOT等试验技能,一个完整的Ex Vivo药效学试验需要试验人员两方面能力均要有熟练度的要求,对人员和平台的复合能力要求较高。
6. 方法学验证和数据汇报体系设计。Ex Vivo药效学试验无明确的指导原则,由于其非定量试验类型,不能完全按照PK方法的参数进行验证,由于其存在个体差异,也不能完全按照免疫原性的参数进行验证,如何设计一个合适的方法学验证体系来证明或者表征方法的精密度,灵敏性,特异性,稳固性,稳定性,基质效应等参数,确保能够满足真实样品的检测需求,需要基于多方面的考量。
综上所述,Ex Vivo药效学分析方法是难度非常大的分析方法,从方法的设计,方法学开发和方法学验证,对人员和平台均需要有较高的熟练度和经验需求,需要有专业化团队进行完成。
基于药物作用机理的了解和广泛的文献资料的检索调研,熙宁生物专业化的Ex Vivo药效学评估团队能够为客户的早期临床药物提供个性化的临床药效学评估解决方案,加速临床研发进度,助力临床药物研发的精细化管理,欢迎咨询讨论。

Accurant BioTech
熙宁生物
熙宁生物是一家专业的符合国际GLP&GCP质量管理规范的大分子生物分析实验室,为国内外生物医药公司提供临床和临床前大分子生物分析(Bioanalysis,BA) 和伴随诊断(Companion Diagnostics,CDx) 产品开发服务。
一站式的生物分析服务包括抗体制备和细胞株构建,样本采集包及实验室手册,符合法规要求的分析方法学的开发和验证,以及样本分析。
涵盖药代动力学(PK),药效动力学(PD),抗药抗体(ADA),中和抗体(NAb),和生物标志物(Biomarker)检测。包括基于流式细胞术(FACS)和荧光定量PCR (qPCR) &数字PCR(dPCR)平台针对细胞治疗药物(如CAR-T,CAR-NK)和基因治疗药物的PK, PD分析服务,以及细胞和基因水平的生物标志物检测服务。
伴随诊断产品开发服务包括LDT方法学开发、CDx产品开发及验证、注册检验、临床试验研究和注册申报。
公司核心技术团队有10-25年的专业经验,有多位在国际知名药企和CRO任职多年的海归博士、大分子生物分析专家、中美多个行业协会的常任理事,曾参与《中国药典2015版》“生物样品分析方法验证指导原则”、2021年NMPA《药物免疫原性研究技术指导原则》、及国际上多个行业白皮书的撰写,支持过200多项全球多中心临床试验,100多个各类大分子产品的临床研究,为多个国际重磅级药物提供上市审批数据支持,多次成功通过FDA、EMA、OECD、NMPA的审计。
公司在宁波(熙宁生物)、上海(精翰生物)、和美国新泽西(Accurant Bio)都建有实验室,总面积超过6,500 平方米,科学家团队规模超过150人。已经和国内外近百家药企和生物科技公司建立了临床和临床前研究的项目合作,涵盖肿瘤免疫,自身免疫,降糖等多个热门治疗领域,包含蛋白药物,基因及细胞治疗药物等各类生物大分子,其中双特异性抗体>15个,基因和细胞治疗药物>28个,在研靶点>40个,临床试验>180个。成功支持了国内第一款一类新药的Car-T产品-药明巨诺倍诺达®(瑞基奥仑赛注射液)的上市。
公司地址:
上海:上海市外高桥自由贸易试验区加枫路8号5楼、7楼
宁波:宁波市高新区聚贤路587弄A5幢4楼、8楼
美国:259 Prospect Plain Road, Building H, Suite168, Cranbury, New Jersey, USA
网址:www.accurantbio.com
公司邮箱:customer-services@accurantbio.com
联系方式:0574-87878487

- END -
下一篇:阿兹夫定:中国审评报告出炉!
 药融圈社群
药融圈社群


 您现在的位置:
您现在的位置:



