Tu如其来!脱发(斑秃)新药全球首次获批
脱发是普遍困扰中年人,尤其是中年男性的一个棘手问题,由此催生出的植发、假发行业更是风生水起。据国家卫健委发布数据,我国超2.5亿人饱受脱发的困扰,平均每6人中就有1人脱发,而且“90后”脱发比例高达84%,比上一代的脱发年龄提前了20年,且低龄化趋势明显。
脱发主要包括雄激素性脱发(AGA)和斑秃(AA,Alopecia Areata)等几类,其中雄激素性脱发(AGA)是由于对雄激素的过度反应而在遗传上预先确定的疾病,特征是在青春期后头皮的终毛逐渐脱落,约占整体脱发的90%。目前获批治疗AGA脱发的药物有限,仅有米诺地尔和非那雄胺。
斑秃(AA)是一种会造成头皮、面部、有时进行性累及身体其他部位斑块状毛发脱落的自身免疫性疾病。斑秃常常在患者儿童时期首次发病,不同患者的首次发病情况有所不同。各个年龄、性别及人种均有可能出现斑秃。流行病学研究显示我国AA的患病率为0.27%,国外研究显示人群终生患病率约2%。
巴瑞替尼(baricitinib)是一款每天一次口服给药的JAK抑制剂,在全球超过70个国家和地区获批用于治疗中重度活动性类风湿关节炎(RA)成年患者。在中国获批的适应症为适用于对一种或多种改善病情抗风湿药(DMARD)疗效不佳或不耐受的中重度活动性类风湿关节炎成年患者。巴瑞替尼可以与甲氨蝶呤或其他非生物改善病情抗风湿药联合使用。

2009年12月,礼来制药与因赛特医疗(Incyte)宣布了针对巴瑞替尼研发、商业化以及相关后续化合物针对炎症性疾病、自身免疫性疾病的全球独占专利和合作协议。
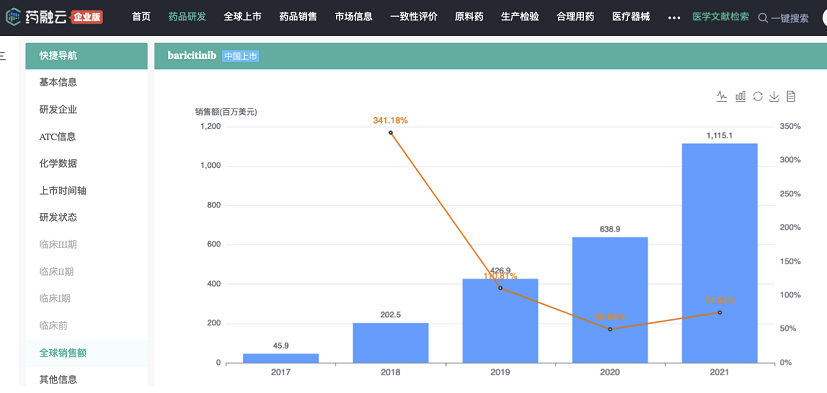
药融云数据 www.pharnexcloud.com;近几年本品全球业绩
2021年10月,礼来与Incyte披露针对1200名重度斑秃患者进行的两项Ⅲ期临床试验BRAVE-AA1和BRAVE-AA2的结果,这是目前已完成主要终点的最大的Ⅲ期临床研究项目。研究将重度斑秃定义为脱发重度程度工具 (SALT) 评分≥50(头皮脱发面积大于等于50%)。研究主要终点是在第36周,受试者SALT ≤20(即 80% 或更多头皮毛发覆盖)的患者比例。在这两项研究中,大约三分之一接受剂量为4 mg的巴瑞替尼治疗的患者达到头皮毛发覆盖面积超过80%(BRAVE-AA1=35.2%,BRAVE-AA2=32.5%),而安慰剂组的数值分别为5.3%(BRAVE-AA1)和2.6%(BRAVE-AA2)。
与服用安慰剂的患者相比,在使用巴瑞替尼 4mg 治疗36周后,有三分之一的患者实现了眉毛和睫毛的完全再生或再生,而这些患者在基线时均有明显的缝隙或没有明显的眉毛或睫毛。(BRAVE-AA1:4mg 剂量:眉毛=31.4% [n=59];睫毛=33.5% [n=56];安慰剂:眉毛=3.2% [n=4];睫毛=3.1% [n=3] ; BRAVE-AA2:4mg 剂量:眉毛=34.8% [n=56];睫毛=34.3% [n=48];安慰剂:眉毛=4.5% [n=5];睫毛=5.6% [n=5] ];对于与安慰剂的所有比较,p≤0.001)。眉毛和睫毛脱发是使用临床医生报告的结果 (ClinRO) Measure for Eyebrow Hair Loss™ 和由礼来公司开发的经过临床验证的新型工具 ClinRO Measure for Eyelash Hair Loss™ 进行评估的。
同时,BRAVE-AA Ⅲ 期临床项目还评估了艾乐明®的安全性,没有观察到新的安全性信号。研究中很少有患者因不良事件而停止治疗(两项研究中为 2.6% 或更少),并且大多数治疗出现的不良事件的重度程度为轻度或中度。
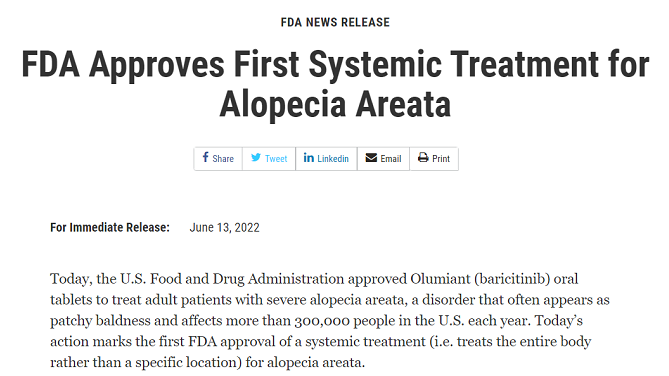
2022年6月13日,美国FDA宣布,批准巴瑞替尼(baricitinib)上市,用于治疗严重斑秃成人患者,这是FDA批准用于治疗斑秃的首款系统性疗法。此外,欧盟获批在即:欧洲药品管理局人用医药产品委员会支持其巴瑞替尼获批用于治疗重度斑秃成人患者。日本监管机构正在审评新药上市申请。
中国斑秃诊疗指南,临床皮肤科杂志.2020,49(2)69—72.;等等。
<END>
 药融圈社群
药融圈社群


 您现在的位置:
您现在的位置:



