神经退行性疾病深耕者Denali勇攀“险峰”:跨越血脑屏障
神经退行性疾病
神经退行性疾病是当前存在重大未满足需求的医疗领域之一。随着老龄化进程的加快,这类疾病已成为日趋沉重的医疗和社会负担。以痴呆症(Dementia)为例,据统计,全世界约有5000万人患有痴呆症,预计到2050年,这一数字将增长到1.52亿,阿尔茨海默病(AD)是痴呆症最常见的形式,可能占痴呆症病例的60~70%。
这类疾病往往是由神经元结构或功能的进行性丧失引起,最终会导致神经细胞死亡,且目前没有已知的方法可以逆转神经元的进行性退化,所以神经退行性疾病被认为是无法治愈的,就连能够减缓疾病进展的手段也是极少。神经退行性疾病发病机制复杂,具体病因仍未明晰,个体的临床表现和生理学特征存在异质性,这不但为临床诊疗带来巨大障碍,也使这类疾病的新药开发成功率奇低,甚至被视为“研发黑洞”。
血脑屏障成为“致命”障碍
近年来,随着针对神经退行性疾病机制研究的不断深入,与之相关的多种通路和靶点相继被发现,如ApoE、tau蛋白、IGF-1、HIF-1、α-突触核蛋白、TREM2等。不过,这些新治疗靶点的出现并未对这个领域的药物开发带来实质性突破,其中一个重要的问题就是血脑屏障(Blood-BrainBarrier, BBB)的存在。
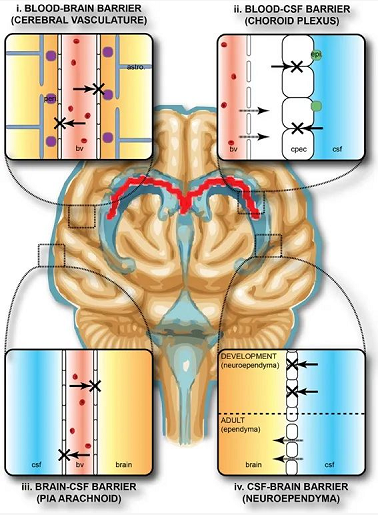
▲血脑屏障示意图源:Front.Integr.Neurosci.|
https://doi.org/10.3389/fnint.2013.00061
BBB是介于血液和脑组织之间对物质具有选择性透过作用的动态界面,由内皮细胞、星形胶质细胞末端和周细胞组成,该系统对于维持大脑的微环境并保护其免受血液中循环有害物质和病原体的侵害至关重要,但也使大多数药物无法在大脑中达到有效治疗浓度,将98%的小分子药物以及100%的大分子神经治疗药物阻挡在大脑之外,为神经退行性疾病的治疗带来巨大挑战。
前基因泰克高管创立,Denali创新技术突破血脑屏障
Denali Therapeutics是一家专注于神经退行性疾病的生物制药公司,据了解,该公司由前基因泰克(Genentech)的高管Ryan Watts、Marc Tessier-Lavigne以及Alex Schuth联合创立,并以北美最高峰‘Denali’(德纳里)命名,昭示着这家公司不凡的勇气与野心。Ryan Watts博士曾在基因泰克领导了神经科学领域方面的研究,实现大分子跨越血脑屏障也是他努力了十多年的方向。

药融圈旗下,药融云数据www.pharnexcloud.com显示,自成立之时,该公司已获多次融资,投资方包括Baillie Gifford、Flagship Pioneering、ARCH Venture Partners、Alaska Permanent Fund等。
Denali公司开发了专有的转运载体(Transport Vehicle,TV)技术平台,能够使治疗用生物大分子更有效地穿过血脑屏障,包括酶、抗体、蛋白质和寡核苷酸。2020年5月,这项创新技术由Science Translational Medicine同期的两篇文章进行了报道,并引起一阵轰动,意味着数十年致力于突破血脑屏障的研究终于取得了可喜进展。

该技术基于工程化的Fc片段,该片段与BBB上特定的天然转运受体,如转铁蛋白受体(TfR)相结合,并通过受体介导的胞吞作用穿过BBB,从而将治疗用生物大分子传递到大脑。该平台已在小鼠和非人类灵长类动物模型中进行了安全性和药代动力学/药效学效果的概念验证。与传统的抗体治疗相比,利用TV技术进行静脉给药的抗体可在大脑中产生强大且持续的药效学效应,在亨特综合征(Hunter综合征)小鼠模型中,运用该技术向脑部递送IDS酶可显示出强大且持续的效果。为了支持多种生物大分子的递送,TV技术目前已衍生出了ATV(抗体转运载体)、ETV(酶转运载体)、PTV(蛋白转运载体),以及OTV(寡核苷酸转运载体)平台。
值得一提的是,该转运载体技术平台的开发基于Denali与F-star Gamma于2016年8月达成的合作,合作旨在利用F-star的模块化抗体技术与Denali在神经退行性疾病领域的专业知识,共同开发可实现跨BBB药物递送的Fc片段。2018年5月,Denali收购F-star Gamma,使其成为Denali的全资子公司,并将其实体名称更改为Denali BBB Holding Limited。
科学策略驱动,攀登神经退行性疾病“险峰”
尽管神经退行性疾病领域存在极大的未满足医疗需求,但目前这类患者几乎没有有效的治疗选择。为了提高药物开发的成功率并更快地为患者提供有效疗法,Denali Therapeutics为药物开发工作制定了三个科学策略。
利用遗传通路的潜力——根据那些将人类遗传变异与患神经退行性疾病风险相联系的研究,来选择治疗靶点和疾病通路。这些研究确定了特定基因突变会导致神经退行性疾病,或成为神经退行性疾病的主要危险因素,该公司将这类基因称为“退行相关基因(Degenogenes)”。
工程化脑部递送技术——利用实现跨血脑屏障递送的工程化技术设计候选产品,使药物直接作用于脑部。
生物标志物驱动药物开发——发现、开发并利用生物标志物来选择合适的患者群体,指示疾病途径或靶点的结合程度,以及候选产品对疾病进展的影响。
在研产品管线
药融圈旗下,药融云数据www.pharnexcloud.com显示,目前Denali Therapeutics在研候选产品中已有6款进入临床试验阶段,另有超过15个处于临床前开发阶段的项目,适应症涉及帕金森病(PD)、亨特综合征(MPSII,黏多糖贮积症II型)、肌萎缩侧索硬化症(ALS)、多发性硬化症(MS)、阿尔茨海默病(AD)、额颞叶痴呆(FTD)等等,主要合作伙伴包括渤健Biogen、武田Takeda、赛诺菲Sanofi。

▲Denali临床/申报临床阶段管线(更新至2022年5月)
自2007年以来,神经退行性疾病相关基因的研究迅速增长,得益于测序技术的飞速发展,科学家能够筛选出与疾病相关的信号通路和可能的重要治疗靶点。Denali认为,“退行相关基因”在疾病信号通路中起着重要作用,当这些通路失调时,个体患神经退行性疾病的风险则会增加。这些基因和信号通路为药物开发计划的优先次序提供了强有力的科学基础。目前该公司药物开发项目专注于调节三个关键疾病途径:溶酶体功能、神经胶质细胞、细胞稳态。
溶酶体功能途径:
溶酶体系统功能障碍与多种神经退行性疾病有关,包括帕金森病、溶酶体贮积症(LSD)引起的神经退行性疾病。与溶酶体功能相关的“退行相关基因”包括富含亮氨酸重复激酶2(LRRK2)、颗粒蛋白前体(PGRN)、α-突触核蛋白(aSyn),以及溶酶体酶,如艾杜糖醛酸-2-硫酸酯酶(IDS)、磺酰胺酶(SGSH)和葡萄糖脑苷脂酶(GBA)。
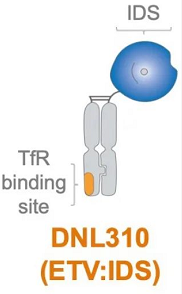
DNL310(ETV:IDS)是Denali利用TV技术平台开发的重组IDS酶产品,旨在跨越血脑屏障用于治疗亨特综合征(MPSII,黏多糖贮积症II型)。该产品是Denali使用TV技术平台开发的主打项目,也是公司科学策略的典型代表,并在2020年11月首次实现TV技术的人类生物标志物概念验证。2022年2月,Denali宣布DNL3101/2期临床试验新的长期数据,支持每周静脉给药DNL310可作为一种差异化酶替代疗法,快速使脑脊液(CSF)中硫酸乙酰肝素(HS)水平正常化,并使CSF溶酶体功能生物标志物实现持续的改善。该产品预计将在2022年上半年开启2/3期临床试验。
BIIB122(DNL151)是一款靶向LRRK2的小分子抑制剂,由Denali与Biogen合作开发,用于治疗帕金森病。LRRK2是帕金森病最常见的遗传风险因素,其水平升高会引起溶酶体功能障碍,从而导致神经变性和路易体的形成,这是帕金森病的核心病理学特征。2021年5月,公司宣布针对BIIB122开展的1期和1b期临床研究均达到了安全性和生物标志物的目标。目前,BIIB122正在由Biogen主导开展全球2b期LUMA试验以及全球3期LIGHTHOUSE试验。(Denali针对帕金森病的LRRK2小分子抑制剂项目并非其原研,而是在2016年6月从基因泰克获得独家授权。)
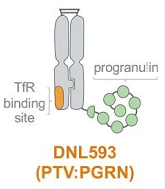
DNL593(PTV:PGRN)是利用TV技术平台开发的重组颗粒蛋白前体(PGRN),旨在穿过血脑屏障并进入大脑中的多种细胞类型,以治疗因PGRN缺乏导致的额颞叶痴呆(FTD)。该产品由Denali与武田合作开发,2022年3月已启动针对FTD-GRN的1/2期研究。
神经胶质细胞途径:
“退行相关基因”还与阿尔茨海默病和其他神经退行性疾病患者大脑的免疫功能障碍有关。这类基因包括髓系细胞触发受体2(TREM2)以及炎性小胶质细胞(大脑的常驻免疫细胞)中高度表达的许多其他基因。例如,受体相互作用丝氨酸/苏氨酸蛋白激酶1(RIPK1)是肿瘤坏死因子(TNF)受体通路下游的一种激酶,在炎性的小胶质细胞和大脑中的其他细胞中过度活跃。
DNL788(SAR443820)是一款靶向RIPK1的小分子抑制剂,可以穿过血脑屏障,目前由Denali与赛诺菲合作开发,用于治疗肌萎缩侧索硬化症(ALS)、多发性硬化症(MS)以及阿尔茨海默病(AD)。RIPK1是肿瘤坏死因子受体通路中的关键信号蛋白,是炎症和细胞死亡的调节因子,大脑中RIPK1活性的增加会引起神经炎症和细胞坏死,从而导致神经退行性变。(美国科学院院士袁钧瑛教授是RIPK1领域的开拓者,其在2005年发现的Necrostatin-1s(Nec-1s)是第一个RIPK1小分子抑制剂。袁钧瑛教授后来将Nec-1s授权给制药公司Incro Pharmaceuticals,该公司已被Denali收购。)目前,赛诺菲正在主导开展DNL788治疗ALS的2期HIMALAYA试验,并计划在MS患者中启动一项2期临床试验。药融云数据www.pharnexcloud.com显示,该产品在国内的IND申请已被CDE承办。(相关阅读:赛诺菲:RIPK1抑制剂报临床,退行性疾病的新锐靶点)
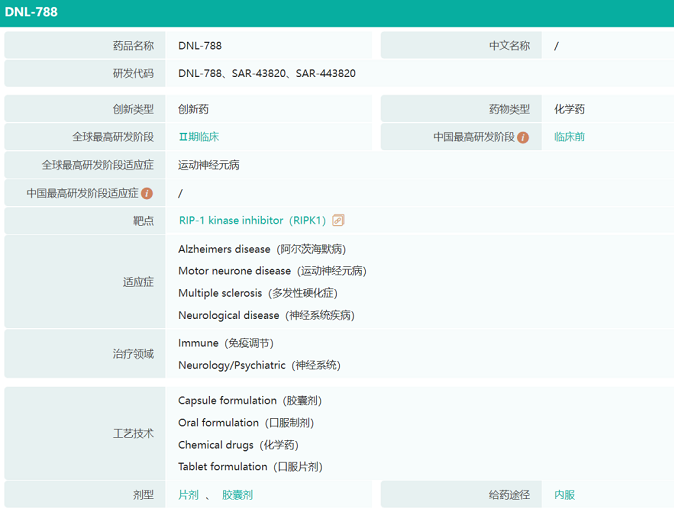
▲截图自药融云数据库
DNL919(ATV:TREM2)是Denali利用TV技术平台开发的靶向TREM2的抗体,用于治疗阿尔茨海默病,目前由Denali和武田合作开发。该产品旨在调节TREM2蛋白的水平,从而使小胶质细胞功能正常化,TREM2基因突变与神经炎症和阿尔茨海默病风险增加密切相关。2022年1月,公司宣布DNL919的IND申请已被FDA搁置,目前正在进一步处理FDA关于临床前毒理评估的观察结果,预计首次人体给药将比原计划推迟至少3个月。

细胞稳态途径:
大脑尤其容易受到脂质、蛋白质或RNA稳态缺陷的影响。一些肌萎缩侧索硬化症(ALS)和额颞叶痴呆(FTD)的“退行相关基因”突变会改变RNA稳态并增加细胞应激。例如,真核起始因子2B(eIF2B)是细胞应激的重要调节因子,eIF2B活性调节因子已被证明在许多体外和体内神经退行性疾病模型中有益。其他与细胞稳态相关的“退行相关基因”还包括淀粉样前体蛋白(APP)、Tau和ApoE。
DNL343是一款具有脑渗透性的小分子eIF2B激活剂,被开发用于治疗肌萎缩侧索硬化症(ALS),公司预计将在2022年年中公布该药治疗ALS的1b期28天治疗数据,以支持推进该产品的后期开发计划。
其他:
DNL758(SAR443122)也是一款靶向RIPK1的小分子抑制剂,但具有外周限制性,不能穿过血脑屏障,同时也是Denali与赛诺菲的合作开发项目,用于治疗自身免疫性疾病。目前,赛诺菲正在主导开展DNL758治疗皮肤红斑狼疮(CLE)的2期临床试验,以及治疗溃疡性结肠炎(UC)的2期临床试验。
财务状况
自成立以来,Denali Therapeutics还没有产品上市销售,截至2022年3月31日,公司累计赤字为7.102亿美元。公司迄今为止所有收入均来自与合作伙伴(武田、赛诺菲、渤健)的合作与许可收入。2021年,公司全年合作收入4866万美元,同比减少86%;研发支出2.653亿美元,同比增长25%;一般及行政开支7906万美元,同比增长31%;公司全年净亏损2.906亿美元。
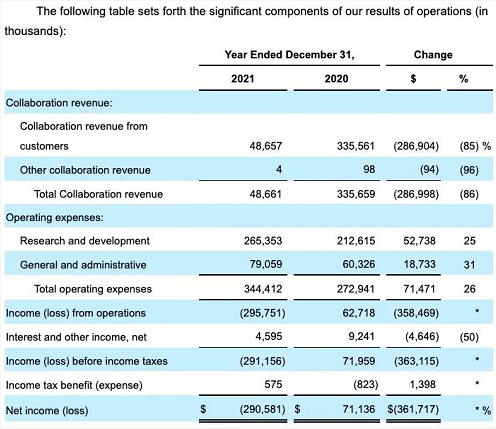
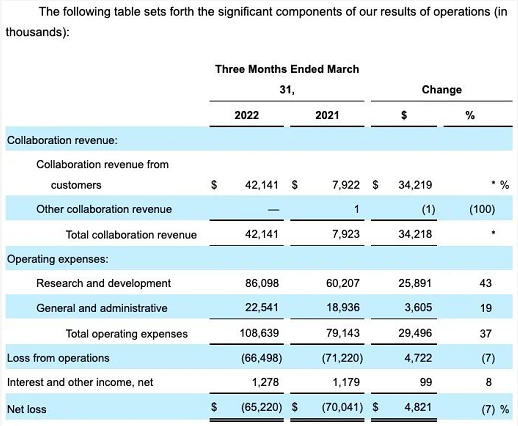
2022年第一季度,公司合作收入4214万美元;研发支出8610万美元,同比增长43%;一般及行政开支2254万美元,同比增长19%;公司第一季度净亏损6522万美元。
截至2022年3月31日,该公司拥有现金、现金等价物和有价证券共约12亿美元。
结 语
神经退行性疾病新药开发成功率之低,让许多大型药企都望而却步,尤其阿尔茨海默病药物的开发在很长时间里都是屡战屡败。近几年,行业里有不少声音对现行的假说和靶点提出质疑,但又苦于没有新的机制来为研究指出准确的方向,像Denali这类既依托现有机制又深耕于创新递送技术的企业或许可以带来新的思路。‘Denali’这一名字意味着抗击神经退行性疾病的艰巨挑战,但新的科学见解和技术带来了前所未有的机遇,对于Denali公司而言,‘TheTime is Right’。

▲图源:DenaliNational Park and Preserve
发送DNLI(请正确复制)至药融圈微信公众号(扫描下方二维码)后台可获得Denali Therapeutics企业展示PDF原文件。仅供学习交流分享!


此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场
参考:
NMPA/CDE;
药融云数据,www.pharnexcloud.com;
FDA/EMA/PMDA;
相关公司公开披露(正文图片除标注外,均来自企业官方);
https://www.denalitherapeutics.com/home;
ErkkinenMG, Kim MO, Geschwind MD. Clinical Neurology and Epidemiology of theMajor Neurodegenerative Diseases. Cold Spring Harb Perspect Biol.2018;10(4):a033118. Published 2018 Apr 2.doi:10.1101/cshperspect.a033118;
LivingstonG, Huntley J, Sommerlad A, et al. Dementia prevention, intervention,and care: 2020 report of the Lancet Commission. Lancet.2020;396(10248):413-446. doi:10.1016/S0140-6736(20)30367-6;
PraveenBallabh, et al,The blood–brain barrier: an overview: Structure,regulation, and clinical implications,Neurobiology ofDisease,https://doi.org/10.1016/j.nbd.2003.12.016.;
Denaliunveils new way of crossing blood brain barrier as the bigneuroscience bet enters its clinical years| Endpts News;
https://www.who.int/zh/news-room/fact-sheets/detail/dementia
http://www.ircbc.ac.cn/view.do?id=1157;等等。
<END>
 药融圈社群
药融圈社群


 您现在的位置:
您现在的位置:



